Las proteínas son moléculas esenciales que representan alrededor del 15-20% de la masa corporal y desempeñan roles fundamentales en prácticamente todos los procesos biológicos. Su estructura única permite una amplia variedad de funciones, desde la construcción de tejidos hasta la regulación metabólica.
¿Qué Son las Proteínas?
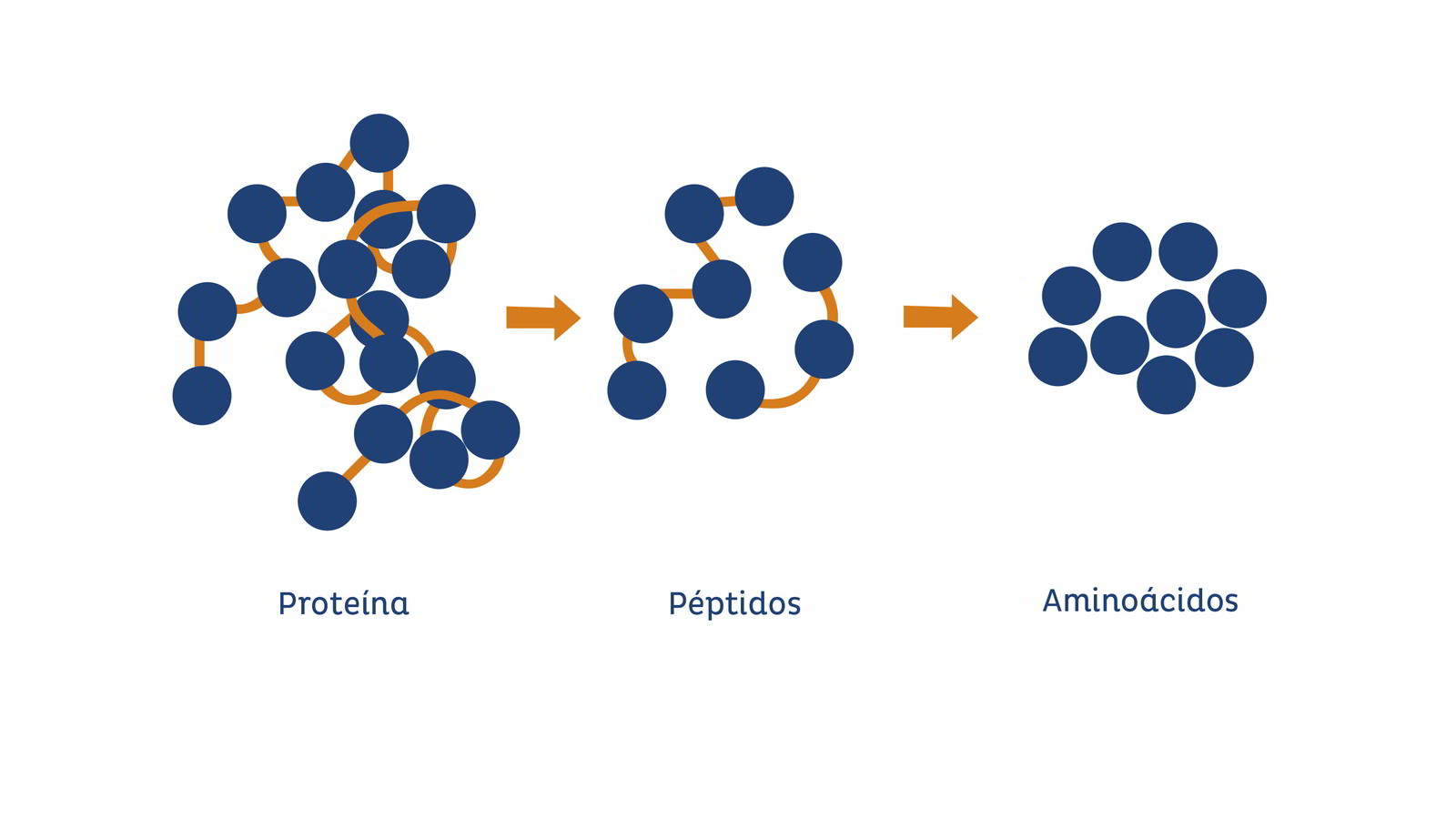
Las proteínas son macromoléculas compuestas por cadenas lineales de aminoácidos, que se unen mediante enlaces peptídicos. Existen 20 aminoácidos estándar, de los cuales 9 son esenciales y deben obtenerse de la dieta. Cada proteína tiene una secuencia específica de aminoácidos determinada por el ADN, lo que le confiere su forma tridimensional única.
La estructura de las proteínas se organiza en cuatro niveles:
- Primaria: Secuencia lineal de aminoácidos.
- Secundaria: Estructuras locales como hélices alfa o láminas beta, estabilizadas por puentes de hidrógeno.
- Terciaria: Plegamiento tridimensional global, mantenido por interacciones hidrofóbicas, puentes disulfuro y enlaces iónicos.
- Cuaternaria: Asociación de múltiples cadenas polipeptídicas, como en la hemoglobina.
Esta complejidad estructural es clave para su funcionalidad específica; un cambio mínimo (mutación) puede alterar drásticamente su rol, como ocurre en enfermedades como la anemia falciforme.
Estructura Molecular Detallada
La estructura primaria actúa como el blueprint genético. Por ejemplo, la insulina tiene 51 aminoácidos en dos cadenas unidas por puentes disulfuro. La secundaria involucra patrones repetitivos: las hélices alfa representan el 30% de las estructuras proteicas en promedio.
En la terciaria, el núcleo hidrofóbico se forma por residuos no polares, mientras que los polares quedan expuestos para interacciones con agua o ligandos. La cuaternaria es evidente en enzimas multiméricas, donde subunidades cooperan, como en la lactato deshidrogena.
Estas estructuras no son estáticas; muchas proteínas son dinámicas, adoptando conformaciones múltiples para funciones reguladas, un fenómeno conocido como “wobble” o fluctuación conformacional.
Funciones Estructurales
Las proteínas estructurales proporcionan soporte y forma a células y tejidos. El colágeno, la proteína más abundante (30% del total proteico), forma fibras triples en tendones, ligamentos y piel, ofreciendo resistencia a la tracción. Su triple hélice de cadenas ricas en glicina y prolina es única.
La queratina, insoluble y rica en cisteína, endurece uñas, cabello y cuernos mediante puentes disulfuro. La actina y miosina forman filamentos en músculos, permitiendo contracción mediante deslizamiento.
En membranas celulares, proteínas integrales como la rhodopsina mantienen la fluidez y actúan como canales iónicos.
Funciones Enzimáticas y Catalíticas
Las enzimas, casi todas proteínas, aceleran reacciones químicas hasta 10^6 veces. Su sitio activo, un bolsillo conformacional, se adapta al sustrato (modelo “llave-molde” o inducido). La hexoquinasa, por ejemplo, fosforila glucosa en glicólisis.
Sin enzimas, procesos vitales como la digestión (amilasa, pepsina) o replicación ADN (ADN polimerasa) serían imposibles. Muchas requieren cofactores como el hierro en la catalasa.
Transporte y Almacenamiento
La hemoglobina, con cuatro subunidades, transporta oxígeno en eritrocitos mediante su grupo hemo. La albúmina sanguínea lleva ácidos grasos y hormonas. La ferritina almacena hierro en hígado y bazo.
Estas proteínas regulan la homeostasis, distribuyendo nutrientes y eliminando desechos vía glomerular.
Regulación Hormonal y Señalización
Hormonas proteicas como la insulina (70 aa) regulan glucosa sanguínea; su deficiencia causa diabetes. El factor de crecimiento epidérmico (EGF) estimula proliferación celular.
Neurotransmisores proteicos y receptores GPCR median señales neuronales y hormonales.
Defensa Inmunológica
Los anticuerpos (inmunoglobulinas) son proteínas en Y con regiones variables que reconocen antígenos. La IgG neutraliza patógenos; las citoquinas como interferón coordinan respuestas inmunes.
El complemento, un sistema proteico, lisa bacterias.
Fuentes y Requerimientos Diarios
Se obtienen de carnes, huevos, lácteos (completas), legumbres y cereales (incompletas, combinables). Adultos necesitan 0.8-1.2 g/kg/día; atletas hasta 2 g/kg. Deficiencia causa kwashiorkor; exceso sobrecarga renal.
Beneficios para la Salud y Ejercicio
Post-ejercicio, proteínas activan mTOR para síntesis muscular (MPS). BCAA como leucina estimulan recuperación. En envejecimiento, previenen sarcopenia.
Enfermedades Relacionadas con Proteínas
Plegamientos erróneos causan Alzheimer (amiloide) o Parkinson (alfa-sinucleína). Mutaciones en cisteína alteran queratina en piel.